解答と解説
1.
(1)A…炭酸ナトリウム B…水 C…二酸化炭素
(2)炭酸水素ナトリウム水溶液より、Aの水溶液のほうが赤色がこくなった
(3)青色から赤(桃)色に変化した
(4)黄色
(5)水の逆流をふせいで試験管を割らないようにするため
(6)B…1.8g C…4.4g
|
参考ページ…分解 質量保存の法則 指示薬一覧
炭酸水素ナトリウムの熱分解の問題です。
反応前後の物質全体の質量が変わらないということも問題にしています。
(1)
炭酸水素ナトリウムは熱すると
炭酸水素ナトリウム(白い固体)→炭酸ナトリウム(白い固体)+水(液体)+二酸化炭素(気体)
に分解します。
(2)
フェノールフタレイン溶液はアルカリ性だと赤色になります。
炭酸水素ナトリウム水溶液も炭酸ナトリウム水溶液もアルカリ性ですが、炭酸ナトリウム水溶液のほうが強いアルカリ性です。
よって、炭酸ナトリウム水溶液(Aの水溶液)のほうが赤色がこくなります。
(3)
水の検出には塩化コバルト紙が使われますね。水があると、青色から赤(桃)色に変化します。
(4)
二酸化炭素は水に少しとけて酸性を示します。BTB溶液を加えると酸性では黄色ですね。
(5)
この実験の注意はテストに出やすいです。
ガラスは急激な温度変化に弱いです。急に冷やされると割れてしまいます。
液体からガラス管を抜く前に火を消してしまうと、液体が熱い試験管の中に逆流してきて、試験管が急に冷えて割れて危険です。
先にガラス管を抜いて、ガラス管の先端を空気中に出してしまえば、試験管の中には空気が入ってくるだけなので安心ですね。
|
★水が逆流する理由★(参考) 参考ページ…アンモニアの噴水実験
熱せられて試験管内の空気が膨張
↓
ここで火を消すと、試験管内の温度が下がって空気が縮む(試験管内の気圧が下がる)
↓
縮んだぶんの空気が占めていた体積ぶんを埋めようと水が入ってくる
|
(6)
反応前後で物質全体の質量は保存されます。
固体A(炭酸ナトリウム)と液体B(水)と気体C(二酸化炭素)を合わせた質量は、16.8gになるはずですね。
「ゴム栓+試験管」の質量は、57.4(g)−16.8(g)=40.6(g)
実験後の全体の質量が53.0gなら、「固体A+液体B」の質量=53.0(g)−40.6(g)=12.4(g)
固体Aは10.6gなので、液体B(水)の質量=12.4(g)−10.6(g)=1.8(g)
A+B+Cの質量=16.8(g)より、
気体C(二酸化炭素)の質量=16.8(g)−10.6(g)−1.8(g)=4.4(g)
2.
(1)A…H2 B…O2
(2)ポンと音をたてて燃える
(3)イ
(4)2H2O→2H2+O2
(5)イとエ
|
参考ページ…分解 化学式 化学反応式のつくり方
水の電気分解だということに気がつけば楽勝です。
純粋な水は電流を通さないため、少量の水酸化ナトリウムをとかして電気分解しましたね。
(1)
陰極には水素、陽極には酸素が発生します。
「水素」「酸素」は物質名なので、化学式で答えましょう。
水素(A)の化学式はH2、酸素(B)の化学式はO2ですね。
(2)
水素の性質ですね。この程度の水素の量なら、ポンと音がして燃える(爆発する)程度です。
(3)
発生する水素と酸素の体積比は2:1です。水素が10cm3発生したら、酸素はその半分の5cm3(イ)ですね。
(4)
化学反応式のつくり方のとおり、2H2O→2H2+O2 ですね。
(5)
ちょっと難しいかもしれません。
本当はなぜ水酸化ナトリウム自体が電気分解されないで水が分解されるのかを知らないと推測できませんが、少量の硫酸(イ)や硫酸ナトリウム(エ)も水酸化ナトリウムの代わりになることを覚えておきましょう。
水が分解される理由の参考ページ…イオン(参考)>電気分解>水の電気分解(参考)
塩酸を電気分解すると塩素と水素が発生します。
塩化銅水溶液を電気分解すると塩素が発生し、銅が析出します。
3.
(1)分解
(2)酸化銀
(3)酸素原子
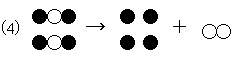
|
参考ページ…分解 分子をつくるもの 化学反応式のつくり方
酸化銀の分解のようすをモデルで考えます。
(1)
1種類の物質が2種類以上の違う物質に変化する化学変化は分解ですね。
(2)
●はAg(銀原子)、○2個が結びついたものは助燃性があるということから酸素分子です。
●(銀原子)が2個、○(酸素原子)が1個の割合で結びついているのは酸化銀(Ag2O)です。
(3)
○は酸素原子を表します。
「O」は酸素の原子記号で、酸素原子自体を示すこともありますが、原子記号なのでこの場合は不可です。
また、「酸素」は物質名(物質の種類を表す名前)または元素名(その原子1種類で作られた単体を示す物質名)で、特定の1個の原子を表すものではありません。
(4)
反応前後で原子の種類と数は変化しません。
酸化銀をもう1個、銀をもう1個かき足して、→の両辺とも銀原子4個・酸素原子2個としておきましょう。
この反応を化学反応式で表すと、
2Ag2O → 4Ag + O2 となります。
top
> 実戦問題解説 > 2年 > 分解