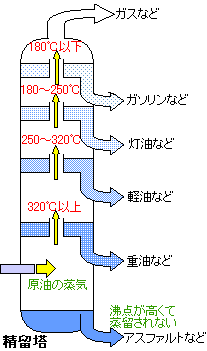
エタノールも水も純粋な物質ですが、お互いを混ぜ合わせると混合物です。この混合物からエタノールをとり出す実験ですね。
|
手順
エタノール3cm3と水17cm3を混ぜ、 出てきた液体を2cm3ずつ試験管 それぞれの試験管の液体について
|
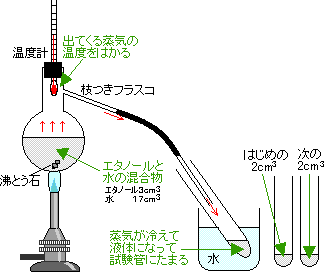 |
結果
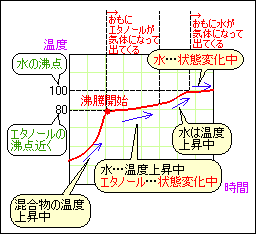
グラフでは、沸点がはっきりしませんが、エタノールの沸点付近の温度で少し水平に近い部分を探します。
そこが混合物の中のエタノールが沸騰している部分です。
|
1本め(エタノールの沸点くらいの温度) 2本め 3本め(水の沸点くらいの温度) |
 |