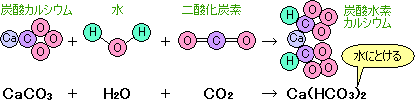2年生では化学反応式を習います。
反応前の物質と反応後の物質とのつくりの関係がわかりやすく表せますので、化学変化後にどうしてその物質ができたか、理解しやすいです。
ここでは、気体に関する化学反応式を集めて紹介しておきます。このページは2年生の化学反応式を習ってから参考にしてください。
このページで登場する化学反応式は中学では習いませんが、反応前後の物質の化学式だけわかれば中学生でも化学反応式をつくる練習にはなります。
なお、物質のモデルは、各原子の数の確認のためにつくったもので、実際の物質のつくりと形が異なることがあります。
気体の発生に関する化学反応式
前ページにて中学で覚えるべき気体の発生方法の一例を紹介しましたが、その方法でどうして気体が発生するのか気になる方は以下を参考にしてください。
※モデルで、反応前後のそれぞれの種類の原子の数が同じであることを確認してください。
二酸化炭素と石灰水
二酸化炭素を石灰水に通すと白くにごる、というのは有名で大事な性質ですね。
これは「二酸化炭素と石灰水が反応して、水にとけない白い沈殿ができた」という状況です。
なお、石灰水は水酸化カルシウムの水溶液です。
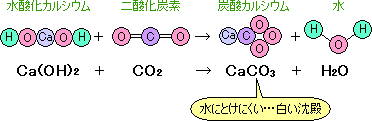
炭酸カルシウムは水にとけにくい白い物質なので、石灰水が白くにごります。
さらに二酸化炭素を通すと、炭酸カルシウムと水と二酸化炭素が化合して炭酸水素カルシウムができます。
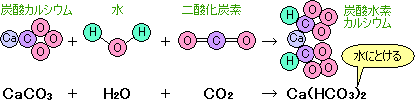
炭酸水素カルシウムは水にとけてしまうので、あまり二酸化炭素を通しすぎると、また石灰水は透明になってしまうのです。
top
> 身のまわりの物質 > 気体 > 気体に関する化学変化(参考)